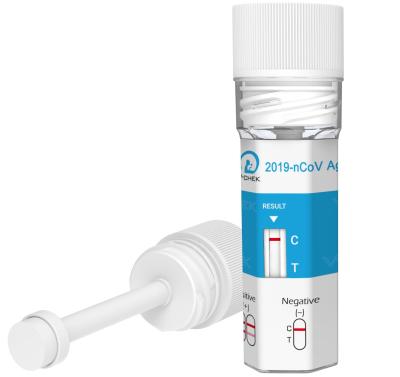
tasse 2019 rapide d'essai de salive de nCoV AG
Avis
Le produit est pour à usage unique seulement ; ne le réutilisez pas. Dispose of a employé le produit, les échantillons et d'autres consommables en tant que déchets médicaux selon des règlements applicables.
En raison de la protection sanitaire et des raisons hygiéniques, il n'est pas possible de renvoyer les marchandises dans les 15 jours. Le vendeur se réserve le droit de livrer aux marchandises d'acheteur du fabricant identique, de la même chose ou des meilleurs paramètres/conception (par exemple en raison du remplacement par une nouvelle variante avec un groupe différent de nom ou de production).
DESCRIPTION
Essai rapide sans écouvillon de nez ou de gorge
Appliquez-vous à l'avant de la bouche pendant 90 secondes
Résultat d'essai après la minute 15
Sensibilité : 95,65%
Spécificité : 98,44%
approprié au l'auto-essai - même avec des enfants
application simple
CE certifié
BfArM a énuméré
PRINCIPE DE L'ESSAI
Cet essai emploie le sandwich à double-anticorps pour détecter légalement l'antigène du syndrôme respiratoire aigu grave nouveau (2019-nCoV) dans des échantillons de salive. Pendant la détection, l'or a marqué l'anticorps monoclonal d'anti-2019-nCoV dans les grippages de étiquetage de protection à l'antigène 2019-nCoV dans l'échantillon pour former un complexe, et le complexe de réaction se déplace en avant le long de la membrane de nitrocellulose sous l'action de la chromatographie, il est capturé par l'anticorps monoclonal d'anti-2019-nCoV enduit d'un préenduisage par la zone de détection (t) sur la membrane de nitrocellulose, et finalement une ligne rouge de coloration est formée dans la zone de T. Si l'échantillon ne contient pas l'antigène 2019-nCoV, une ligne rouge de coloration ne peut pas être formée dans la zone de T. Indépendamment de si l'échantillon examiner contient l'antigène 2019-nCoV, une ligne rouge de réaction formera toujours dans le secteur de contrôle de qualité (c).
MATÉRIAUX ET COMPOSANTS
Matériaux équipés d'essai
UTILISATION PRÉVUE
La tasse d'essai est un immunoessai latéral d'écoulement destiné à la détection qualitative du nCoV d'antigène de protéine de nucleocapsid à partir de 2019 - dans des spécimens de salive directement rassemblés des personnes qui sont suspectées de COVID-19 par leur fournisseur de soins de santé moins de les 7 premiers jours du début de symptôme.
Les résultats sont pour l'identification de l'antigène de protéine du nucleocapsid 2019-nCoV. Les résultats positifs indiquent la présence des antigènes viraux, mais la corrélation clinique avec l'histoire patiente et toute autre information diagnostique est nécessaire pour déterminer le statut d'infection. Les résultats positifs n'éliminent pas l'infection bactérienne ou la Co-infection avec d'autres virus. L'agent a détecté peut ne pas être la cause définie de la maladie.
Des résultats négatifs devraient être traités comme présumés, et n'éliminent pas l'infection 2019-nCoV et ne devraient pas être employés comme base unique pour le traitement ou les décisions de gestion patientes, y compris des décisions de contrôle d'infection. Des résultats négatifs devraient être considérés dans le cadre des expositions récentes d'un patient, de l'histoire, et de la présence des signes cliniques et des symptômes compatibles à COVID-19, et être confirmés avec une analyse moléculaire s'il y a lieu, pour la gestion patiente.
La tasse d'essai est prévue à l'usage du personnel clinique qualifié de laboratoire a spécifiquement instruit et a formé des procédures de diagnostic in vitro.
RÉSUMÉ ET EXPLICATION
Les syndrômes respiratoires aigus graves nouveaux appartiennent au genre de β. COVID-19 est une maladie infectieuse respiratoire aiguë. Les gens sont généralement susceptibles. Actuellement, les patients infectés par le syndrôme respiratoire aigu grave nouveau sont la source d'infection principale ; les personnes infectées asymptomatiques peuvent également être une source infectieuse. Basé sur l'enquête épidémiologique actuelle, la période d'incubation est de 1 à 14 jours, en grande partie 3 à 7 jours. Les manifestations principales incluent la fièvre, la fatigue et la toux sèche. L'obstruction nasale, l'écoulement nasal, l'angine, la myalgie et la diarrhée sont trouvés dans quelques cas.
PRINCIPE DE L'ESSAI
Ce réactif emploie le sandwich à double-anticorps pour détecter légalement l'antigène du syndrôme respiratoire aigu grave nouveau (2019-nCoV) dans des échantillons de salive. Pendant la détection, l'or a marqué l'anticorps monoclonal d'anti-2019-nCoV dans les grippages de étiquetage de protection à l'antigène 2019-nCoV dans l'échantillon pour former un complexe, et le complexe de réaction se déplace en avant le long de la membrane de nitrocellulose sous l'action de la chromatographie, il est capturé par l'anticorps monoclonal d'anti-2019-nCoV enduit d'un préenduisage par la zone de détection (t) sur la membrane de nitrocellulose, et finalement une ligne rouge de coloration est formée dans la zone de T. Si l'échantillon ne contient pas l'antigène 2019-nCoV, une ligne rouge de coloration ne peut pas être formée dans la zone de T. Indépendamment de si l'échantillon examiner contient l'antigène 2019-nCoV, une ligne rouge de réaction formera toujours dans le secteur de contrôle de qualité (c).
MATÉRIAUX ET COMPOSANTS
Matériaux équipés de kits d'essai
| Caractéristiques Ingrédients | 0599U4X001 | 0599U4X05 | 0599U4X010 | 0599U4X015 | 0599U4X020 |
| Tasse d'essai | 1 | 5 | 10 | 15 | 20 |
| Écouvillon de salive | 1 | 5 | 10 | 15 | 20 |
| Instructions pour l'usage | 1 | 1 | 1 | 1 | 1 |
| Instructions de référence rapide | Na | 1 | 1 | 1 | 1 |
Note : Les composants dans différentes séries du kit ne peuvent pas être mélangés.
Matériaux requis mais non fournis
STOCKAGE ET STABILITÉ
- Stockez la tasse d'essai comme emballée entre 2-30°C.
- La tasse d'essai est stable jusqu'à la date d'échéance imprimée sur l'emballage externe.
- N'employez pas au delà de la date d'échéance.
- Ne gelez aucun contenu de l'essai
- La tasse d'essai doit rester dans la poche scellée jusqu'à l'utilisation.
CONDITIONS D'ÉCHANTILLON
- Insérez l'extrémité d'éponge de l'écouvillon de salive dans la bouche. Tamponnez activement l'intérieur de la bouche et de la langue pour rassembler le fluide oral pendant 3 minutes.
- Enlevez l'écouvillon de salive de la bouche quand l'éponge pour devenir entièrement saturé et le rouge de tour d'inducteur.
- Ne mangez ou ne buvez pas aucune chose pendant 4 heures avant l'essai
- Les échantillons devraient être employés dès que possible après rassemblé.
- Des échantillons ne devraient pas être inactivés.
PROCÉDURE D'ESSAIS
Avant essai, lisez svp les instructions soigneusement.
- Prenez la tasse d'essai pour équilibrer à la température ambiante.
- Déballez le sac de papier d'aluminium, placez la tasse d'essai horizontalement sur la table et marquez-la.
- Insérez l'écouvillon de salive dans la tasse d'essai et vissez le chapeau.
- Serrez le couvercle et commencez la minuterie.
- Comme l'essai commence à fonctionner, le mouvement pourpre de couleur à travers la fenêtre de résultat au centre du dispositif d'essai.
- Attente 15 minutes et lire les résultats. Ne lisez pas les résultats après 20 minutes.
INTERPRÉTATION DES RÉSULTATS D'ESSAI
Ce produit peut seulement exécuter l'analyse qualitative sur l'objet de détection.
Résultat positif :
Si les lignes de C et de T sont évidentes d'ici 15 minutes, le résultat d'essai est positif et valide.
Note : Les spécimens contenant les niveaux très bas des anticorps de cible peuvent développer deux discriminations raciales plus de 15 minutes.
Résultat négatif :
Si la zone d'essai (ligne de T) n'a aucune couleur et la zone de contrôle montre une discrimination raciale, le résultat est négatif et valide
Résultat invalide :
Le résultat d'essai est invalide si une discrimination raciale ne forme pas dans la région de contrôle. L'échantillon doit être retesté, utilisant une nouvelle tasse d'essai.
LIMITATIONS
- Le résultat de la tasse d'essai ne devrait pas être pris comme diagnostic confirmé, pour la référence clinique seulement. Le jugement devrait être fait avec des résultats de RT-PCR, des symptômes cliniques, l'information épidémiologique et encore d'autres données cliniques.
- La performance de tasse d'essai dépend de la quantité de virus (antigène) dans l'échantillon et peut ou peut ne pas se corréler avec des résultats viraux de culture effectués sur le même échantillon.
- La tasse d'essai doit être équilibrée à la température ambiante (18℃~26℃) avant utilisée, autrement les résultats peuvent être incorrects
- Un résultat d'essai négatif peut se produire si le niveau de l'antigène dans un échantillon est au-dessous de la limite de détection de l'essai.
- Le manque de suivre la procédure d'essais peut compromettre la représentation d'essai et/ou infirmer le résultat d'essai.
- Réagissez moins de 15 minutes peuvent mener un résultat de faux négatif ; Réagissez plus de 15 minutes peuvent mener un résultat de faux positif.
- Les résultats d'essai positifs n'éliminent pas des Co-infections avec d'autres agents pathogènes.
- Des résultats d'essai négatifs ne sont pas prévus pour ordonner dans d'autre viral ou infections bactériennes.
- Des résultats négatifs devraient être traités comme présumé et être confirmés avec une analyse moléculaire.
- La représentation clinique avait lieu a évalué avec les échantillons frais.
- Les utilisateurs devraient examiner des spécimens aussi rapidement que possible après collection de spécimen.
CARACTÉRISTIQUE DE FONCTIONNEMENT
1. Vérification clinique
La performance de la tasse d'essai a été établie avec l'échantillon 232 rassemblé des patients symptomatiques, qui avec le début de symptômes d'ici 7 jours.
Sensibilité : 95,28% (101/106), CI de 95% (89,43, 97,97)
Spécificité : 98,41% (124/126), CI de 95% (94,40, 99,56).
| tasse rapide d'essai de salive de 2019-nCoV AG (Immunochromatography) | Résultat d'essai comparatif de RT-PCR |
| Positif (+) | Négatif (-) | Total |
| Positif détecté | 101 | 2 | 103 |
| Négatif détecté | 5 | 124 | 129 |
| Total | 106 | 126 | 231 |
La performance de la tasse d'essai avec des résultats positifs stratifiés par les comptes comparatifs du seuil de cycle de méthode (Ct) ont été rassemblées et évalué pour comprendre mieux la corrélation de la performance d'analyse au seuil de cycle, comme présenté dans la table ci-dessous, l'accord positif de la tasse d'essai est plus haut avec des échantillons d'un compte <25 de Ct.
| tasse rapide d'essai de salive de 2019-nCoV AG (Immunochromatography) | RT-PCR comparatif Méthode (Positif par valeur de Ct) |
| Positive>25 (Ct<=25) | Positif (Ct>25) |
| Positif détecté | 80 | 21 |
| Total | 81 | 25 |
| Accord positif | 98,76% | 84,00% |
2. Limite de détection
Les résultats expérimentaux prouvent que pour la concentration de culture de virus au-dessus de 100 TCID50 /mL, le taux positif de détection est supérieur ou égal à 95%. Pour la concentration en culture de virus de 50 TCID50 /mL et ci-dessous, le taux positif de détection est inférieur à 95%. Ainsi, la limite de la détection de la tasse d'essai est 100 TCID50 /mL.
3. Activité hétérospécifique
L'activité hétérospécifique de la tasse d'essai a été évaluée. Les résultats n'ont montré aucune activité hétérospécifique avec le spécimen suivant.
4. substances d'interférence
Les résultats d'essai ne sont pas interférés la substance à la concentration suivante :
1. L'essai 10 replie de négatif et de positif à l'aide des documentations de référence des entreprises. L'accord négatif et l'accord positif étaient 100%.5. Précision
2. Kits différents de sorts de l'essai trois comprenant les documentations de référence positives et négatives des entreprises. Les résultats négatifs et les résultats positifs étaient 100%
6. Effet de crochet
La tasse d'essai était jusqu'à 1,6 le × examiné 105 TCID50 /ml de la tension 2019-nCoV chaleur-inactivée et aucun effet de haut-dose n'a été observé.
PRÉCAUTIONS
- Pour l'usage diagnostique in vitro.
- Employez les précautions appropriées dans la collection, la manipulation, le stockage, et la disposition des échantillons patients et avez employé le contenu d'essai.
- L'utilisation des nitriles, gants de latex (ou équivalent) est recommandée en manipulant les échantillons patients.
- Ne réutilisez pas l'écouvillon utilisé de tasse ou de salive d'essai.
- Devrait ne jamais ouvrir la poche d'aluminium de la tasse d'essai l'exposition de elle à l'environnement ambiant jusqu'à ce que la tasse d'essai soit prête pour l'usage immédiat.
- Jetez et n'employez pas n'importe quelle tasse ou matériel d'essai endommagé ou laissé tomber.
- La collection témoin, le stockage, et le transport insuffisants ou inadéquats peuvent donner des résultats d'essai faux.
- Collection témoin et procédures de manipulation exiger la formation et les conseils spécifiques.
- Pour obtenir des résultats précis, n'employez pas les échantillons visuellement ensanglantés ou excessivement visqueux.
- Pour obtenir des résultats précis, une tasse ouverte et exposée d'essai ne devrait pas être utilisée.
- L'essai devrait être réalisé dans un secteur avec la ventilation adéquate.
- Portez les vêtements de protection, les gants, et la protection appropriés d'oeil/visage en manipulant le contenu de cet essai.
- Mains de lavage complètement après manipulation.
CLÉ AUX SYMBOLES UTILISÉS
| Matériaux inclus | | | Tasse d'essai | |
| Instructions pour l'usage | | | Écouvillon de salive |
| Consultez les instructions Pour l'usage | | | Datez de Fabricant |
| Magasin à 2°C~30°C | | | Ne réutilisez pas |
| Date d'échéance | | | Numéro de catalogue |
| Fabricant | | | Gardez à partir de la lumière du soleil |
| Numéro de lot | | | Essais par kit |
| Gardez au sec | | | Dispositif médical diagnostique in vitro |
| | Biotechnologie Cie., Ltd de Guangzhou Decheng Pièce 218, bâtiment 2, No.68, route de Nanxiang, ville de la Science, secteur de Huangpu, 510000, Guangzhou P.R.China Téléphone : +86-020-82557192 sales@dochekbio.com www.dochekbio.com | |
| Dispositifs médicaux et drogues S.L. de CMC. C/ Horacio Lengo Nº 18, CP 29006, Málaga, Espagne | |
Doc no : DC-IN-0599C01 Ver 1,0
Rel. : 2020/12/01